Kambario temperatūros natrio jonų baterijų atgaivinimas
Dėl gausios natrio (Na) atsargų Žemės plutoje ir panašių natrio bei ličio fizikinių ir cheminių savybių natrio pagrindu pagamintas elektrocheminis energijos kaupimas žada didelį energijos kaupimą ir tinklo plėtrą. Pavyzdžiui, aukštos temperatūros nulinės emisijos baterijų tyrimų elementai, pagrįsti Na / NiCl2 sistemomis ir aukštos temperatūros Na-S elementai, kurie yra sėkmingi komerciniai stacionarių ir mobiliųjų programų atvejai, jau įrodė natrio pagrindu veikiančių įkraunamų baterijų potencialą. Tačiau jų aukšta, maždaug 300 °C, darbinė temperatūra kelia saugumo problemų ir mažina natrio jonų baterijų (SIB) efektyvumą. Todėl kambario temperatūros (RT) SIB plačiai laikomi perspektyviausia alternatyvia LIB technologija.
Per pastaruosius 200 metų baterijų istoriją SIB tyrimai buvo karštai atliekami kartu su LIB plėtra. Elektrocheminis TiS2 aktyvumas ličiui ir jo galimybė kaupti energiją pirmą kartą buvo iškelta aštuntajame dešimtmetyje. Po šio atradimo devintojo dešimtmečio pradžioje buvo suvokta, kad Na jonai gali būti įterpiami į TiS+2. Grafitą atradus kaip nebrangią ir vidutinės talpos anodo medžiagą LIB ir nepavykus įsiterpti natrio jonų, 1990-aisiais įvyko spartus LIB vystymasis, pakeisdamas natrio chemijos augimą. Tada, 2000 m., galimybė natrio saugojimui kietojoje anglyje (HC), kuris užtikrintų panašią energijos talpą kaip Li grafite, padidino susidomėjimą SIB tyrimais.
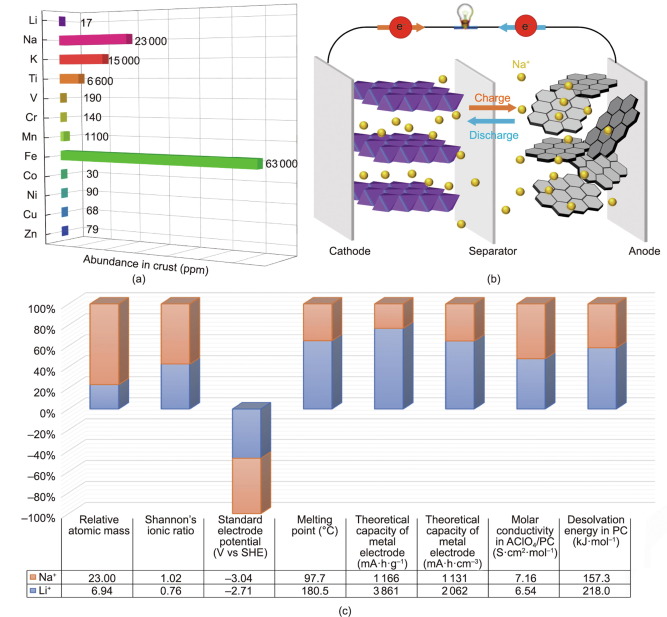
Natrio jonų ir ličio jonų akumuliatorių palyginimas
SIB atgaivinimas kartu su vis didėjančiu spaudimu dėl ličio atsargų trūkumo ir atitinkamai didėjančių sąnaudų suteikia LIB papildomą strategiją. Siekdamos patenkinti didėjančią atsinaujinančios energijos technologijų skverbtį, SIB sulaukė vis didesnio mokslinių tyrimų dėmesio ir esminių medžiagų mokslo pasiekimų. Ląstelių komponentai ir SIB elektrocheminės reakcijos mechanizmai iš esmės yra identiški LIB, išskyrus įkrovimo nešiklį, kurio viename yra Na, o kitame Li. Pagrindinė greito SIB medžiagų chemijos plėtros priežastis yra dviejų šarminių metalų fizikinių ir cheminių savybių paralelės.
Pirma, SIB veikimo principai ir ląstelių konstrukcija yra panašūs į komercinių LIB, nors Na yra krūvio nešiklis. Tipiškame SIB yra keturi pagrindiniai komponentai: katodo medžiaga (dažniausiai Na turintis junginys); anodo medžiaga (nebūtinai turinti Na); elektrolitas (skystoje arba kietoje būsenoje); ir separatorius. Įkrovimo proceso metu natrio jonai išgaunami iš katodų, kurie paprastai yra sluoksniuoti metalų oksidai ir polianijoniniai junginiai, ir tada įterpiami į anodus, o srovė per išorinę grandinę teka priešinga kryptimi. Išsikrovimo metu Na palieka anodus ir grįžta į katodus procesu, kuris vadinamas „sūpamosios kėdės principu“. Šie panašumai leido iš anksto suprasti ir sparčiai augti SIB technologiją.
Be to, didesnis joninis Na spindulys turi savų pranašumų: padidina elektrocheminio pozityvumo lankstumą ir sumažina desolvatacijos energiją poliniuose tirpikliuose. Didesnis jonų spindulio tarpas tarp Li ir pereinamojo metalo jonų paprastai sukelia medžiagų konstrukcijos lankstumo gedimą. Priešingai, natrio pagrindu sukurta sistema suteikia lankstesnių kietų struktūrų nei ličio pagrindu pagaminta sistema ir turi didžiulį joninį laidumą. Tipiškas pavyzdys yra β-Al2O3, kurio Na interkalacija turi puikų dydį ir didelį laidumą. Daugiau sluoksniuotų pereinamųjų metalų oksidų su skirtingais M + x + krovimo būdais galima lengvai realizuoti natrio pagrindu veikiančioje sistemoje. Panašiai, daugybė kristalų struktūrų, žinomų dėl natrio jonų laidininkų (NaSICON) šeimos, yra daug sudėtingesnės nei ličio analogų. Dar svarbiau, kad NaSICON junginiuose gali būti leidžiamas daug didesnis jonų laidumas, kuris gerokai viršija ličio jonų laidininko (LiSICON) junginių jonų laidumą.
Paskutinis, bet ne mažiau svarbus dalykas, sisteminiai tyrimai su skirtingais aprotiniais poliniais tirpikliais parodė, kad didesnis joninis Na spindulys sukelia silpnesnę desolvatacijos energiją. Mažesnio Li paviršiaus krūvio tankis aplink šerdį yra didesnis nei Na, kai abu turi tą patį valentingumą. Todėl Li yra termodinamiškai stabilizuojamas, dalijantis daugiau elektronų su polinių tirpiklių molekulėmis. Tai reiškia, kad Li gali būti klasifikuojamas kaip Lewis rūgšties rūšis. Dėl to labai poliarizuotam Li reikalinga santykinai didelė desolvatacijos energija, todėl Li transportavimas iš skystos būsenos (elektrolito) į kietą (elektrodą) sukelia santykinai didelį perdavimo pasipriešinimą. Kadangi desolvatacijos energija yra glaudžiai susijusi su perdavimo kinetika, vykstančia skysčio / kietos medžiagos sąsajoje, santykinai maža desolvatacijos energija yra reikšmingas pranašumas kuriant didelės galios SIB.